 |
|
Главная :: Архив статей :: :: Ссылки |
 |
|
Главная :: Архив статей :: :: Ссылки |
Наши друзья Помощь сайту R935344738975 Наша кнопка Партнеры • Чекап в мюнхене. Check up чек в мюнхене www.munich-medical.ru/de/checkup/prevention. |
Архив статей > Химия > Опыты без взрывов > Металлы в школьной лаборатории Металлы в школьной лаборатории Г. Койдан Каждый видел медь, железо, алюминий, но многие ли могут сказать, как выглядит, например, ванадий? Между тем юным химикам вполне по силам получить некоторые металлы из их соединений. Однако для дома такие эксперименты далеко не всегда годятся, их надо проводить в школьной лаборатории (или в химическом кружке) под руководством преподавателя. Чтобы вы не забыли об этом, мы и вынесли это предупреждение в заголовок. И еще одно: вряд ли кобальт, ванадий, сурьма и висмут понадобятся дома, зато очень лестно будет пополнить школьную коллекцию собственноручно полученными и достаточно редкими металлами. СУРЬМА Многие распространенные сплавы свинца содержат немало сурьмы: баббит и твердый свинец для аккумуляторных пластин - около 15%, несколько меньше - охотничья дробь, а вот типографский сплав гарт - целых 25%. Чтобы извлечь сурьму, опилки любого из названных сплавов надо растворить oв азотной кислоте, причем ОБЯЗАТЕЛЬНО ПОД ТЯГОЙ. В колбу емкостью 250 мл налейте 40 мл азотной кислоты и небольшими порциями, по мере растворения, всыпьте 15 г опилок. Поначалу реакция идет медленно, но постепенно кислота разогревается, процесс заметно ускоряется и выделяется бурый газ. В растворе образуются азотнокислые соли свинца и меди, а вот белый осадок на 'дне колбы - это смесь сурьмяной и оловянной кислот. Отделите осадок и промойте его несколько раз водой. (ОСТОРОЖНО: ВОДА ПОСЛЕ ПРОМЫВКИ ЯДОВИТА!) К очищенному осадку добавьте 20 мл 20%-ного раствора едкого натра и по каплям, по избежание разогрева, при постоянном перемешивании - холодный раствор станнита натрия. Несколько слов о том, как приготовить такой раствор. Тут самая трудная часть работы; она требует аккуратности и терпения. 5 г мелких оловянных опилок растворите при нагревании в 50 мл соляной кислоты. Упарьте раствор до 15 мл, охладите и, перемешивая, прибавьте по каплям 30 мл 20%-ного раствора едкого натра. Следите, чтобы при перемешивании температура не превышала 25°С. Когда вы добавите раствор станнита натрия к ранее полученному раствору антимоната натрия, выпадет черный осадок металлической сурьмы. Отфильтруйте его, промойте и высушите. Чтобы получить компактный слиток, порошок следует расплавить в пробирке, нагревая его в присутствии флюса (хлорида цинка) до температуры около 700°С. ВИСМУТ В ветеринарных аптеках продается азотнокислый висмутил BiONO (основной нитрат висмута). Полтора грамма этого вещества прокалите на пламени горелки. Сольразложится до окисла Bi2O3 (красно-коричневого в горячем виде и желтого на холоде). Полученную окись висмута смешайте с 0,3 г порошка древесного угля. При нагревании до температуры 500-600°С окись восстановится до металла. Если взять в качестве флюса канифоль, то из порошка металла можно выплавить королек висмута. КАДМИЙ В живописи используют пигмент кадмий желтый. Если и если вам не удастся достать порошка пигмента, то можно прокалить кадмиевую масляную краску: после того как масло выгорит, останется главным образом сульфид кадмия CdS, то есть собственно пигмент. Поместите в пробирку 1 г пигмента, влейте 1 мл концентрированной серной кислоты и нагрейте ПОД ТЯГОЙ (будет выделяться сероводород) до исчезновения желтой окраски. Охладите и осторожно перелейте раствор в пробирку с 5 мл воды, а затем профильтруйте раствор в другую пробирку, в которую положен кусочек цинка. Через несколько часов на цинке образуется "шуба" из мелких кристаллов металлического кадмия. Таким образом из раствора можно "выудить" практически весь кадмий. Порошок кадмия также можно сплавить в небольшой слиток, используя в качестве флюса канифоль. ХРОМ, ВАНАДИЙ, КОБАЛЬТ, МАРГАНЕЦ И НИКЕЛЬ Все эти металлы можно получить из окислов методом алюмотермии. Окислы СrО3 и V2O5 обычно есть в школьной лаборатории. NiO, CoO и Мn3О4 можно приготовить самостоятельно, разлагая карбонаты. Для этого достаточно растворить 10 г любой растворимой соли никеля, марганца или кобальта в 100 мл воды, смешать со 100 мл 10%-ного раствора соды (Na2CO3), a затем отфильтровать, промыть и высушить выпавший осадок карбоната. При прокаливании карбонатов на воздухе до 300-400°С образуются соответствующие окислы. Смеси для алюмотермии надо составлять ОЧЕНЬ ОСТОРОЖНО, перемешивая на бумаге деревянной палочкой совершенно сухие компоненты в следующих весовых соотношениях:
СЖИГАТЬ ТЕРМИТНУЮ СМЕСЬ МОЖНО ТОЛЬКО В ПОЖАРОБЕЗ-ОПАСНОМ МЕСТЕ, ПОД ТЯГОЙ. НАДЕТЬ ТЕМНЫЕ ОЧКИ! ДЕРЖАТЬСЯ ОТ ГОРЯЩЕЙ СМЕСИ НА БЕЗОПАСНОМ РАССТОЯНИИ! Проще всего проводить реакцию в несложном приспособлении, изображенном на рисунке. 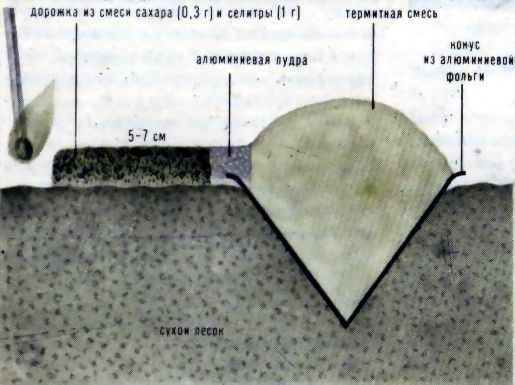 После сгорания термитной смеси в хрупкой массе окисла алюминия нетрудно обнаружить кусочки металла. Еще раз напоминаем: все эти опыты можно ставить только в лаборатории в присутствии преподавателя, соблюдая все указанные меры предосторожности.
Главная :: Архив статей :: :: Ссылки |